科学家揭开困扰科学界数十年谜题:高海拔地区竟能解锁血糖调控的“隐藏开关”
本文是专业学术论文解读,不做医疗建议。
20 世纪 30 年代,哈佛疲劳实验室的研究人员发现了一种奇怪的现象:高海拔地区环境下的人和动物血糖会快速降低。但近一个世纪过去,这背后的机制一直是个“未解之谜”。
直到最近,美国格拉德斯通研究所伊莎·H·贾因(Isha H. Jain)研究员团队在 Cell Metabolism 发表论文 [1],揭示了这种现象的核心机制。
他们发现,红细胞会像微型“海绵”那样吸收血糖。在高海拔低氧条件下,身体会产生更多这样的“海绵”,它们汇聚成一个规模巨大的“葡萄糖缓冲池”。这样,红细胞通过改变代谢方式,不仅提升了细胞向全身组织输送氧气的效率,还起到了控制血糖水平的作用。
科学家们还进一步证明,即使在低氧实验之后,当小鼠恢复到正常的氧气水平,慢性缺氧带来的益处仍可以持续数周至数月。
贾因对媒体表示:“红细胞代表着葡萄糖代谢中一个此前未被充分认识的关键环节,这项研究解决了生理学中一个长期存在的难题,有望为理解如何控制血糖开辟全新的思路。”
 (来源:格拉德斯通研究所)
(来源:格拉德斯通研究所)
贾因是格拉德斯通研究所研究员,同时她还担任 Arc 研究所研究员和加州大学旧金山分校教授。长期以来,她聚焦于研究低氧血症(也称为缺氧)如何影响健康和新陈代谢。
在 2023 年发表在 Cell Metabolism 的一项研究中,该团队观察到,低氧条件下的小鼠血糖水平显著低于正常水平 [2]。也就是说,这些小鼠进食后可以快速消耗葡萄糖。通常来说血糖较低、葡萄糖耐量更好,糖尿病的患病风险可能相对较低。
一种反常的现象是:研究人员给缺氧的小鼠喂食葡萄糖时,它们在极短时间内就在血液中消失了。那么,这些葡萄糖究竟去哪里了?
如果从传统机制去分析,有可能会认为是胰岛素信号传导,通过指示肌肉和脂肪细胞从血液中吸收葡萄糖。但令人惊讶的是,PET/CT 扫描显示,即便对小鼠心脏、大脑、肝脏等主要器官逐一分析,也仅能解释总增量约 30% 的葡萄糖摄取量,而其余近 70% 的葡萄糖去向仍然无法解释。
基于此,研究人员推断一定还有其他机制在发挥作用。他们开始怀疑葡萄糖是被血液中的某个细胞消耗掉了。在另一种成像技术帮助下,研究团队发现,红细胞才是之前缺失的“葡萄糖汇”(注:是指任何能够从血液中吸收并利用大量葡萄糖的物质)。
红细胞主要由血红蛋白组成,是体内数量最多的细胞类型,它们甚至没有细胞核或线粒体。成熟红细胞没有线粒体,无法进行有氧氧化,只能依靠葡萄糖糖酵解供能。
在慢性缺氧的情况下,它们的数量会急剧增加,而红细胞在全身血液中循环流动,传统 PET/CT 扫描并不将血液视为目标器官,因此无法显示这部分葡萄糖摄取。
这项研究带来一种“反常识”的发现:红细胞的作用不仅是“氧气搬运工”,更承担起“血糖清道夫”的责任。为验证这一想法,研究团队通过一些传统方法进行验证,以探究红细胞是否真的是解开谜题的关键。
 (来源:Cell Metabolism)
(来源:Cell Metabolism)
首先,他们通过反复抽取缺氧小鼠的血液,使其红细胞计数维持在正常水平,从而阻止了缺氧引起的红细胞激增。但仅此一项,可使血糖显著回升、接近正常,并逆转低血糖症。
然后,研究人员再“反其道而行之”,将红细胞输注到呼吸普通空气的正常小鼠体内。结果显示,增加红细胞数量显著降低了它们的血糖,成为研究中的关键突破口。
 图丨只有在缺氧条件下成熟的红细胞才会增加 GLUT1 葡萄糖转运蛋白的丰度(来源:Cell Metabolism)
图丨只有在缺氧条件下成熟的红细胞才会增加 GLUT1 葡萄糖转运蛋白的丰度(来源:Cell Metabolism)
有趣的是,在早期实验中,研究人员注意到,缺氧小鼠的红细胞对葡萄糖的摄取量更高,这背后很可能是葡萄糖转运蛋白的增加。
随后,他们利用流式细胞术发现,缺氧小鼠的红细胞中每个细胞的 GLUT1 葡萄糖转运蛋白含量均显著升高。这有些不符合常理,因为成熟的红细胞并没有细胞核,这意味着它们不能转录基因或合成新的蛋白质。
那么,这些额外的 GLUT1 蛋白又是如何产生的?
红细胞由骨髓不断产生,寿命约为几个月。研究人员决定检验在缺氧骨髓中产生的红细胞是否会在发育过程中被编程,通过这种方式产生更多的 GLUT1,并在成熟进入血液循环后维持较高的 GLUT1 转运蛋白水平。
他们连续 3 天用生物素标记小鼠体内所有已存在的红细胞,然后将小鼠转移到低氧环境中。从那时起,研究人员不再进行额外的生物素标记,也就是说,骨髓中新生成的红细胞将呈现未被标记的状态。
4 周后,研究人员将新旧红细胞分离,并测量了它们的 GLUT1 水平。有趣的是,只有新合成的红细胞表现出 GLUT1 上调,而老红细胞则完全没有变化。这表明,红细胞成熟并进入血液循环后,会保留其与生俱来的葡萄糖摄取能力,但缺氧会重编程骨髓,使其产生一批新的、对葡萄糖需求更高的红细胞。
至此,研究人员已了解到葡萄糖如何更快地进入缺氧红细胞,但还不清楚它在红细胞内部会发生什么变化。为了寻找问题的答案,他们给小鼠注射了标记的葡萄糖,并追踪了其在红细胞内的转化过程。
他们发现,缺氧红细胞代谢葡萄糖的速度比正常红细胞快得多,几分钟内就能将其转化为 2,3-二磷酸甘油酸(2,3-DPG),这是调节血红蛋白释放氧气能力的关键分子。而这正是人体在高海拔地区所需要的,即缺氧时组织需要更多的氧气。
 (来源:Cell Metabolism)
(来源:Cell Metabolism)
为了解这一现象的分子机制,该团队与科罗拉多大学安杰洛·达历山德罗(Angelo D'Alessandro)教授和马里兰大学艾伦·多克特(Allan Doctor)教授合作,这两位都是红细胞生物学领域的专家。
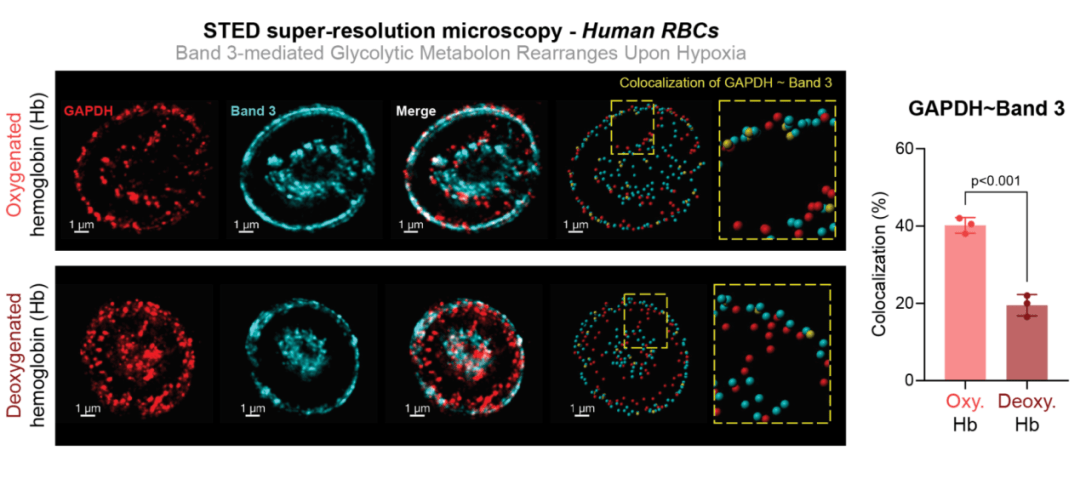
他们发现,在正常氧气条件下,包括 GAPDH 在内的关键糖酵解酶会与蛋白质 Band 3 结合,从而被隔离在红细胞膜上,抑制糖酵解。但当氧气水平下降时,血红蛋白会释放氧气并改变形状。脱氧血红蛋白可以与 Band 3 竞争结合位点,释放糖酵解酶,使其能够合成更多的 2,3-DPG。
该机制将葡萄糖的消耗与氧气的运输巧妙结合,实现了“一举两得”的生理效应。研究人员利用交联蛋白质组学、STED 显微镜和邻近连接分析,在小鼠和人红细胞中证实了这一机制。
 (来源:格拉德斯通研究所)
(来源:格拉德斯通研究所)
为模拟低氧空气的效果,研究人员用贾因团队近期研发的药物 HypoxyStat 进行测试。简单来理解这种药物的作用机制:通过让血红蛋白与氧气更紧密地结合,来阻止氧气到达组织。
结果显示,该药物显著改善高血糖表型(包括 1 型和 2 型糖尿病),甚至比现有药物效果更佳。这种结果为未来开发不依赖传统胰岛素或降糖药的全新疗法,开辟了想象空间。
 图丨相关论文(来源:Cell Metabolism)
图丨相关论文(来源:Cell Metabolism)
“它为我们提供了一种从根本上不同的糖尿病治疗思路——在血糖降低时调动红细胞发挥作用。”贾因说道。
当然,红细胞输注并不是一种治疗糖尿病的理想长期疗法。但这项研究的发现指明了一些潜在的研究方向,例如改造红细胞使其对葡萄糖更具亲和力,或通过调控红细胞周转率来增加红细胞数量,使其更年轻、代谢更活跃。
研究团队还指出,这些发现可能不仅局限于糖尿病,未来也有望应用在运动生理学或创伤后病理性缺氧。尽管这是一个好的开端,但不容忽视的是,仍有许多重要问题需要进一步深入研究。未来他们将继续探索整个身体如何适应氧气变化,并利用该机制探索治疗相关疾病的可能性。
参考资料:
1.https://doi.org/10.1016/j.cmet.2026.01.019
2.https://doi.org/10.1016/j.cmet.2023.02.007
3.https://gladstone.org/news/red-blood-cells-soak-sugar-high-altitude-protecting-against-diabetes
4.https://arcinstitute.org/news/red-blood-cells-glucose-altitude
运营/排版:何晨龙
本文是专业学术论文解读,不做医疗建议。
